“Io credo che il cancro sia una malattia psichica dovuta al fatto che l’individuo che ingoia tutta la sua sofferenza, dopo un certo tempo viene a sua volta ingoiato dal dolore che è dentro di lui.”
— Enzo Soresi
L’intelligenza artificiale sta rivoluzionando la ricerca scientifica in molti settori, incluso lo studio del cancro. In questo articolo, esploreremo il ruolo dell’intelligenza artificiale nell’analisi delle associazioni tra proteine e rischio di cancro, utilizzando i dati della UK Biobank, un ampio database che raccoglie informazioni genetiche e cliniche di oltre mezzo milione di partecipanti. Attraverso l’uso di approcci genetici e algoritmi avanzati, gli scienziati stanno scoprendo potenziali associazioni tra specifiche proteine e diverse tipologie di tumori. Questa nuova metodologia integrata offre nuove prospettive nella comprensione dei meccanismi sottostanti al cancro e potrebbe aprire la strada a nuove terapie mirate.
Le potenziali associazioni tra proteine e rischio di cancro
Le potenziali associazioni tra proteine e rischio di cancro sono un argomento di grande interesse per la ricerca scientifica. Gli studi condotti finora hanno suggerito che alcune proteine possono essere coinvolte nello sviluppo e nella progressione del cancro. Tuttavia, il meccanismo preciso di queste associazioni non è ancora del tutto chiaro. La comprensione di tali legami può essere fondamentale per identificare nuovi biomarcatori diagnostici e terapeutici, nonché per sviluppare strategie preventive efficaci. L’utilizzo dell’intelligenza artificiale nella UK Biobank offre un’opportunità unica per analizzare un vasto insieme di dati genetici e clinici al fine di identificare correlazioni tra specifiche proteine e rischio di cancro. Questo approccio innovativo potrebbe aiutare a identificare nuove vie biologiche coinvolte nella patogenesi del cancro e a sviluppare nuovi trattamenti mirati.
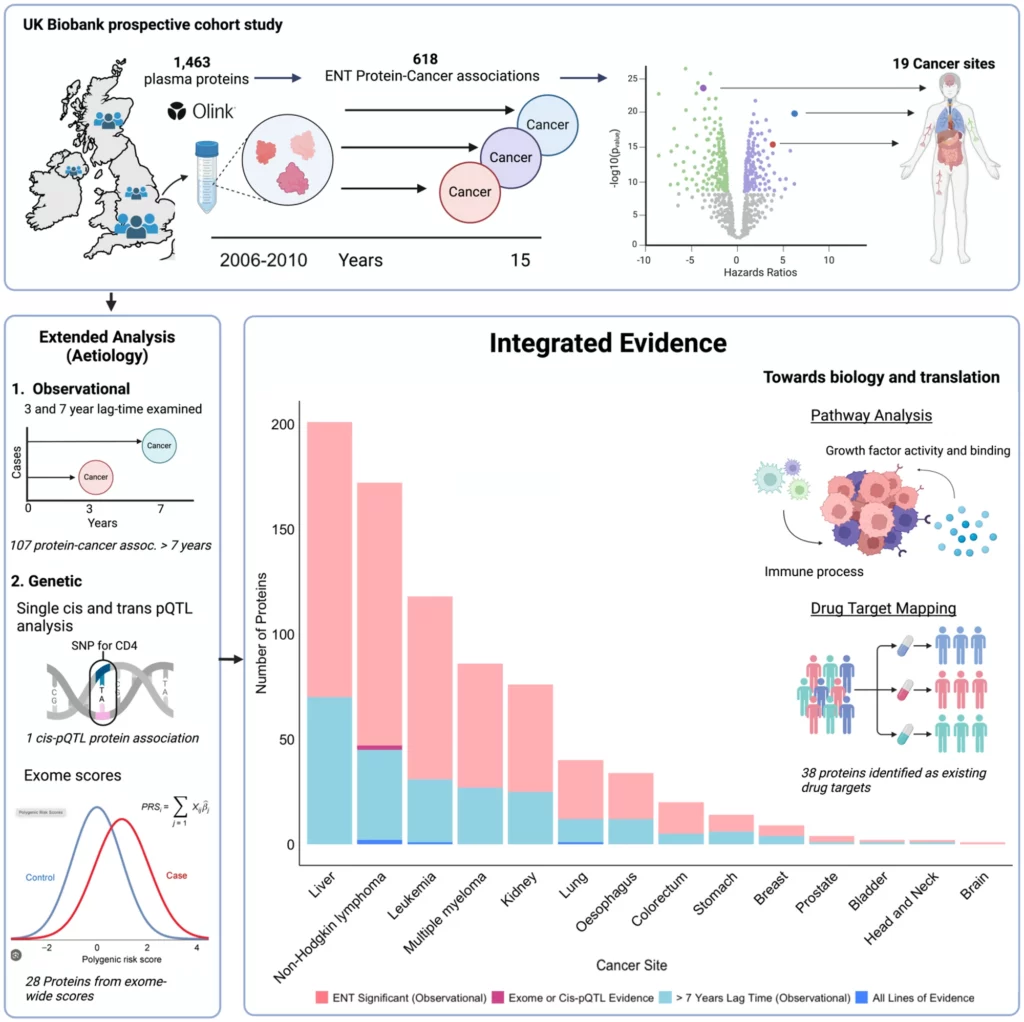
Analisi delle associazioni proteina-cancro nei partecipanti alla UK Biobank
L’analisi delle associazioni proteina-cancro nei partecipanti alla UK Biobank rappresenta un importante campo di ricerca nell’ambito della salute. La UK Biobank è un ampio studio di coorte che coinvolge più di mezzo milione di individui nel Regno Unito, e fornisce una preziosa risorsa per indagare le correlazioni tra le proteine e il rischio di cancro. Grazie all’utilizzo di sofisticate tecniche di analisi, i ricercatori sono in grado di esaminare i dati genetici e clinici dei partecipanti per identificare potenziali associazioni tra specifiche proteine e l’insorgenza di diverse tipologie di tumori. Questo approccio permette di individuare eventuali biomarcatori che potrebbero essere utilizzati per la diagnosi precoce o per lo sviluppo di nuove terapie mirate. L’analisi delle associazioni proteina-cancro nella UK Biobank rappresenta quindi un importante passo avanti nella comprensione dei meccanismi che sottendono lo sviluppo dei tumori e potrebbe aprire la strada a nuove strategie preventive e terapeutiche.
Approcci genetici per approfondire le associazioni proteina-cancro
Gli approcci genetici sono strumenti potenti per approfondire le associazioni tra proteine e rischio di cancro. Attraverso l’analisi del DNA dei partecipanti alla UK Biobank, gli scienziati possono identificare varianti genetiche associate a specifiche proteine coinvolte nello sviluppo del cancro. Queste varianti genetiche, chiamate polimorfismi a singolo nucleotide (SNP), possono fornire informazioni preziose sulla predisposizione genetica al cancro e sulle vie biologiche coinvolte. Utilizzando metodi statistici avanzati, i ricercatori possono valutare l’associazione tra i SNP e il rischio di cancro, fornendo così una comprensione più approfondita dei meccanismi biologici sottostanti. Inoltre, gli approcci genetici consentono di identificare nuovi bersagli terapeutici e di sviluppare trattamenti personalizzati basati sui profili genetici individuali. L’utilizzo dell’intelligenza artificiale nell’analisi dei dati genetici può accelerare ulteriormente la scoperta di associazioni proteina-cancro e migliorare la nostra comprensione del ruolo delle proteine nella patogenesi del cancro.
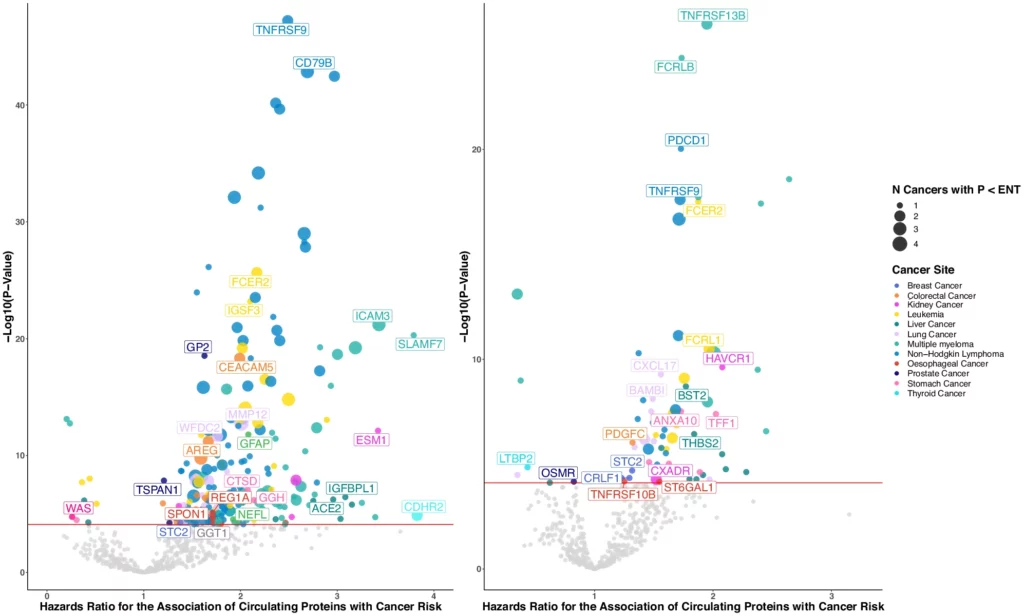
Due diagrammi a vulcano che mostrano i risultati di analisi osservazionali prospettiche di 1463 proteine con rischio di cancro stratificato in base al tempo trascorso dal prelievo alla diagnosi, con analisi tra i casi diagnosticati entro tre anni dal prelievo (a sinistra) e dopo sette anni dal prelievo (a destra). Le principali associazioni proteina-cancro sono rappresentate da punti che indicano il numero di associazioni proteina-cancro ENT significative. Il colore del punto rappresenta la sede del cancro. Gli hazard ratio per il rischio di cancro per SD sono tracciati sull'asse delle ascisse, mentre i p-value -log10 sono tracciati sull'asse delle ordinate. I nomi delle proteine e gli hazard ratio sono etichettati per evidenziare una selezione di associazioni significative dopo la correzione per i test multipli (p < 0,05/639). I rapporti di rischio e gli intervalli di confidenza al 95% per ciascun sito tumorale sono stati stimati separatamente utilizzando modelli di regressione di Cox a rischi proporzionali a due lati. N- numero, ENT - numero effettivo di test. I dati di partenza sono forniti come file di dati di partenza.
Associazioni proteina-cancro persistenti nel tempo
Le associazioni proteina-cancro persistenti nel tempo rappresentano un importante campo di studio per comprendere il ruolo delle proteine nello sviluppo e nella progressione del cancro. Attraverso l’analisi dei dati raccolti dalla UK Biobank, i ricercatori hanno identificato associazioni tra specifiche proteine e il rischio di sviluppare determinati tipi di tumore che si mantengono costanti nel tempo. Queste associazioni persistenti suggeriscono un legame solido tra la presenza di determinate proteine nel corpo e l’insorgenza del cancro. Queste scoperte sono fondamentali per individuare nuovi biomarcatori per la diagnosi precoce del cancro e per sviluppare terapie mirate che possano agire direttamente sulle proteine coinvolte nella malattia. L’utilizzo dell’intelligenza artificiale nell’analisi dei dati della UK Biobank ha permesso di identificare queste associazioni in modo efficiente e accurato, aprendo la strada a ulteriori ricerche sulla relazione tra proteine e cancro.
Un nuovo approccio integrato per comprendere il ruolo delle proteine nel cancro
Nel campo della ricerca sul cancro, un nuovo approccio integrato sta emergendo per comprendere il ruolo delle proteine nella malattia. Gli scienziati stanno utilizzando l’intelligenza artificiale (IA) per analizzare i dati della UK Biobank, un ampio database che contiene informazioni genetiche e di salute di oltre mezzo milione di partecipanti. L’obiettivo è identificare associazioni tra specifiche proteine e il rischio di sviluppare diverse forme di cancro. Grazie all’IA, è possibile analizzare enormi quantità di dati in modo efficiente e identificare correlazioni complesse che altrimenti potrebbero sfuggire all’occhio umano. Questo nuovo approccio integrato offre la possibilità di ottenere una visione più approfondita del ruolo delle proteine nel cancro, aprendo la strada a nuove scoperte e potenziali terapie mirate.
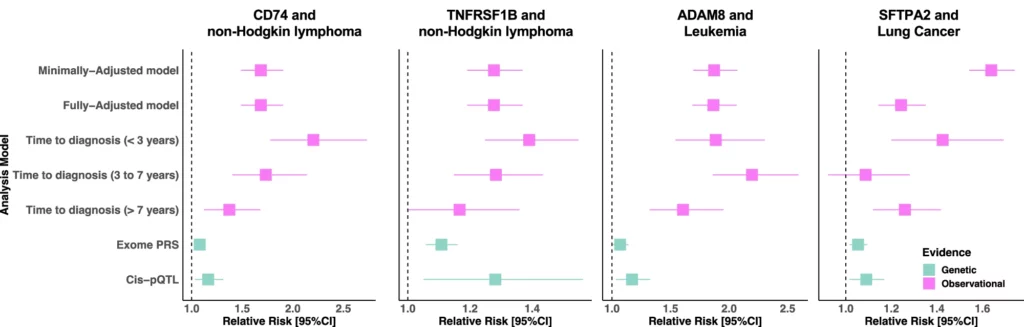
I grafici mostrano le associazioni per le quattro proteine che sono state associate al rischio di cancro nelle analisi principali e che hanno avuto un supporto direzionalmente concordante e convenzionalmente significativo da tutte e tre le analisi aggiuntive, cioè le analisi del tempo di diagnosi lungo (>7 anni), cis-pQTL ed exGS. Per ogni associazione proteina-cancro, l'evidenza dell'associazione delle concentrazioni con il rischio di cancro è presentata da modelli minimamente e completamente aggiustati per SD, così come da modelli stratificati per tempo alla diagnosi, e da analisi del punteggio delle proteine dell'esoma e di cis-pQTL. Le analisi osservazionali (modelli minimamente aggiustati, completamente aggiustati e analisi del tempo alla diagnosi) sono state condotte su un campione massimo di 44.645 partecipanti, mentre le analisi genetiche sono state condotte su un campione massimo di 336.823 partecipanti del Regno Unito. I dati sono presentati come rischio relativo e intervalli di confidenza del 95%. Il valore di riferimento è 1,0. cis-pQTL-cis protein quantitative trait loci. I dati di origine sono forniti come file di dati di origine.
Papier, K., Atkins, J.R., Tong, T.Y.N. et al. Identifying proteomic risk factors for cancer using prospective and exome analyses of 1463 circulating proteins and risk of 19 cancers in the UK Biobank. Nat Commun 15, 4010 (2024). https://doi.org/10.1038/s41467-024-48017-6
In conclusione…
In questo articolo abbiamo esplorato il ruolo dell’intelligenza artificiale nella ricerca delle associazioni tra proteine e rischio di cancro nella UK Biobank. Abbiamo visto come l’analisi delle associazioni proteina-cancro può fornire importanti indicazioni per la prevenzione, la diagnosi e il trattamento del cancro. Gli approcci genetici ci permettono di approfondire ulteriormente queste associazioni e di identificare possibili meccanismi sottostanti. Inoltre, le associazioni proteina-cancro possono essere persistenti nel tempo, fornendo informazioni preziose sulla progressione della malattia. Infine, l’utilizzo di un approccio integrato che combini dati genetici, clinici e molecolari ci aiuta a comprendere meglio il ruolo delle proteine nel cancro. Tuttavia, molte domande rimangono ancora aperte e richiedono ulteriori ricerche. Ad esempio, come possiamo utilizzare queste informazioni per sviluppare nuovi trattamenti personalizzati? Come possiamo tradurre queste scoperte in interventi concreti per migliorare la salute dei pazienti? La continua esplorazione di queste tematiche è fondamentale per progredire nella lotta contro il cancro.





