
“Ciò che dà l’essenza, l’azione e la denominazione ad ogni specie di esseri, o di cose nell’Universo, è appunto la forma di quell’essere o di quella cosa.”
— James Harrington
La cellula sintetica che si adatta rappresenta un passo avanti fondamentale verso nuove frontiere biomediche. Attraverso la creazione di una bolla sintetica capace di imitare la flessibilità delle cellule naturali, i ricercatori stanno aprendo nuove prospettive nel campo della biologia sintetica. Uno dei fenomeni chiave per la vita è la rottura della simmetria, e i progressi nella costruzione di cellule sintetiche hanno permesso di comprendere meglio questo processo fondamentale. Le proteine guida della riorganizzazione cellulare svolgono un ruolo cruciale in questo contesto, aprendo la strada a nuove applicazioni come la somministrazione di farmaci e il rilevamento ambientale.
La bolla sintetica che imita la flessibilità delle cellule naturali
La creazione di una bolla sintetica capace di imitare la flessibilità delle cellule naturali rappresenta un notevole passo avanti nella ricerca biomedica. Questa bolla, realizzata attraverso la costruzione di cellule sintetiche, è in grado di adattarsi e modificarsi come le cellule viventi, aprendo così nuove possibilità per lo sviluppo di terapie e tecnologie innovative. Questa flessibilità è possibile grazie alla rottura della simmetria, un fenomeno fondamentale per la vita stessa. Attraverso progressi significativi nella costruzione di cellule sintetiche, che hanno portato alla creazione del primo batterio sintetico e al movimento cellulare artificiale, si è compreso meglio il ruolo delle proteine guida nella riorganizzazione cellulare. Queste scoperte aprono la strada verso nuove applicazioni, come la somministrazione mirata di farmaci e il rilevamento ambientale.
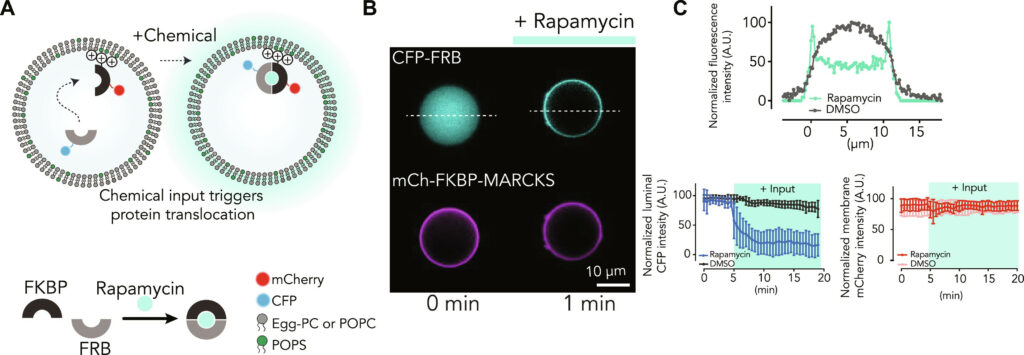
(A) Schema delle GUV contenenti le proteine mCh-FKBP-MARKCS, ancorate alla membrana, e CFP-FRB, luminali. La dimerizzazione di FKBP e FRB indotta dalla rapamicina sposta la proteina CFP-FRB verso la membrana. (B) Immagini di epi-fluorescenza di CFP-FRB (4,4 μM) e mCh-FKBP-MARKCS (7,8 μM) nelle GUV simmetriche contenenti 1-palmitoil-2-oleoil-glicero-3-fosfocolina:1-palmitoil-2-oleoil-sn-glicero-3-fosfo-L-serina (POPC:POPS) (4:1 mol %) nel foglietto lipidico interno. La proteina CFP-FRB, inizialmente luminale, cambia localizzazione verso la membrana pochi minuti dopo la somministrazione di rapamicina. (C) Le scansioni lineari dell'intensità di fluorescenza di mCherry e CFP attraverso la vescicola mostrano la localizzazione della proteina prima e dopo l'aggiunta di rapamicina (in alto). L'intensità di fluorescenza luminale della CFP-FRB (in basso) normalizzata per la media dei valori iniziali prima del trattamento con rapamicina è tracciata, evidenziando la traslocazione su scala minuta della CFP-FRB verso la membrana solo in presenza di rapamicina ma non del veicolo DMSO. Il segnale mCherry associato al marcatore di membrana rimane localizzato nella membrana per tutta la durata dell'esperimento. n = 14 da tre esperimenti indipendenti per entrambe le condizioni di rapamicina e DMSO. Le barre di errore rappresentano la SD. Il riquadro verde indica la presenza di rapamicina. U.A., unità arbitrarie.
La rottura della simmetria: un fenomeno fondamentale per la vita
La rottura della simmetria è un fenomeno fondamentale per la vita. Nell’ambito delle cellule sintetiche, la capacità di rompere la simmetria è un passo cruciale verso l’imitazione delle cellule naturali. Le cellule viventi sono caratterizzate da una struttura asimmetrica, in cui le diverse parti svolgono funzioni specifiche. Questa asimmetria è essenziale per il corretto funzionamento delle cellule e dei tessuti. Nel campo della biologia sintetica, i ricercatori stanno lavorando per sviluppare celle artificiali in grado di riprodurre questa rottura della simmetria. Attraverso l’uso di materiali e tecniche innovative, stanno cercando di creare bolle sintetiche che possano adattarsi e reagire all’ambiente circostante in modo simile alle cellule naturali. La comprensione e l’imitazione di questo fenomeno biologico fondamentale potrebbe aprire nuove frontiere nella ricerca biomedica e nell’applicazione di cellule sintetiche per scopi terapeutici e di rilevamento ambientale.
I progressi nella costruzione di cellule sintetiche: dal primo batterio al movimento cellulare
Negli ultimi anni, la costruzione di cellule sintetiche ha fatto progressi significativi, passando dal primo batterio sintetico al movimento cellulare. I ricercatori sono riusciti a creare una cellula sintetica dotata di un DNA artificiale, aprendo la strada a nuove possibilità nel campo della biologia sintetica. Questa realizzazione ha permesso di comprendere meglio i meccanismi fondamentali che regolano la vita cellulare e ha aperto le porte a nuove applicazioni biomediche. Inoltre, gli scienziati hanno iniziato a sviluppare sistemi in grado di riprodurre il movimento delle cellule naturali. Attraverso l’ingegneria genetica e l’utilizzo di proteine guida, sono stati ottenuti risultati promettenti nella creazione di cellule sintetiche capaci di muoversi autonomamente. Questi progressi nella costruzione di cellule sintetiche pongono le basi per future scoperte nel campo della medicina rigenerativa e dell’ingegneria tissutale.
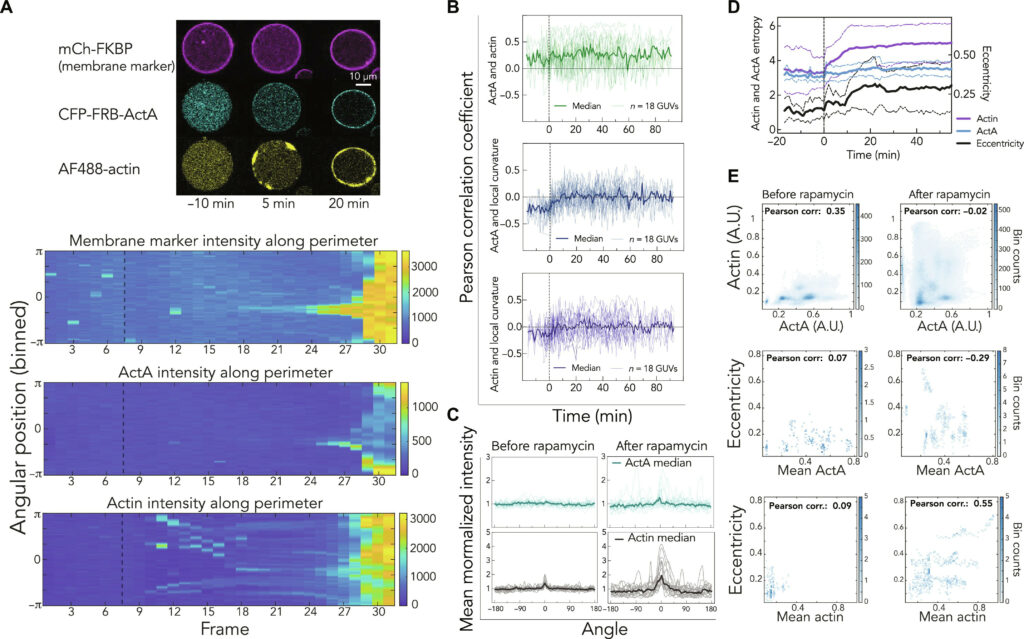
(A) Immagine confocale rappresentativa di una GUV prima e dopo l'aggiunta di rapamicina insieme alle corrispondenti chimografie che tracciano l'arricchimento di ActA e actina sulla membrana nel tempo. t = 0 rappresenta il punto temporale di aggiunta della rapamicina. (B) Il monitoraggio del coefficiente di correlazione di Pearson tra i parametri biochimici (ActA e actina) nel tempo non evidenzia alcun cambiamento di correlazione con l'aggiunta di rapamicina (in alto). L'evoluzione del coefficiente di correlazione di Pearson per ActA e curvatura locale diventa ulteriormente decorrelata con l'aggiunta di rapamicina (al centro). Analogamente, per l'actina e la curvatura locale non si osserva alcuna correlazione (in basso). (C) Profili di intensità di fluorescenza medio-normalizzata di ActA e actina mostrati a due fotogrammi prima della rapamicina e a 10 fotogrammi dopo l'aggiunta di rapamicina. (D) Grafici dell'entropia dei parametri di confine nel tempo, che evidenziano come l'entropia di ActA rimanga costante, mentre quelle di actina ed eccentricità subiscano entrambe un'impennata dopo l'aggiunta di rapamicina. Le barre di errore indicano la SD. (E) Grafici dell'intensità media di ActA, dell'intensità media di actina e dell'eccentricità, dove la correlazione di massa è calcolata sui dati aggregati di tutte le GUV per 18 fotogrammi prima della rapamicina e 35 fotogrammi dopo l'immissione di rapamicina. Per ogni grafico, n = 18 da tre esperimenti indipendenti. La linea nera tratteggiata segna il punto di aggiunta dell'input. Le immagini sono state acquisite alla frequenza di un fotogramma al minuto.
Le proteine guida della riorganizzazione cellulare
Le proteine guida della riorganizzazione cellulare sono fondamentali per il corretto funzionamento delle cellule sintetiche. Queste proteine svolgono un ruolo chiave nel coordinare i processi di movimento e adattamento delle cellule, consentendo loro di rispondere in modo adeguato agli stimoli ambientali. Attraverso complessi meccanismi di segnalazione e interazione con altre proteine cellulari, le proteine guida sono in grado di modulare l’organizzazione e la struttura delle cellule sintetiche. La loro presenza e attività influenzano la flessibilità e la capacità di adattamento delle cellule, permettendo loro di cambiare forma, spostarsi e interagire con il loro ambiente circostante. Comprendere il ruolo e il funzionamento di queste proteine guida è essenziale per sviluppare applicazioni biomediche innovative basate sulle cellule sintetiche, come la somministrazione mirata di farmaci o il rilevamento ambientale.
Verso nuove applicazioni: somministrazione di farmaci e rilevamento ambientale
La cellula sintetica che si adatta rappresenta un importante passo avanti verso nuove frontiere biomediche, in particolare per quanto riguarda le applicazioni nella somministrazione di farmaci e nel rilevamento ambientale. Grazie alla capacità di adattarsi alle diverse condizioni ambientali, queste cellule sintetiche potrebbero essere utilizzate per veicolare specifici farmaci direttamente ai tessuti bersaglio nel corpo umano, aumentando l’efficacia dei trattamenti e riducendo gli effetti collaterali. Inoltre, la flessibilità di queste cellule sintetiche potrebbe consentire loro di essere utilizzate come sensori per rilevare sostanze nocive o contaminanti nell’ambiente. Ciò potrebbe avere un impatto significativo nella sorveglianza ambientale, consentendo una rapida identificazione e risposta a potenziali minacce per la salute pubblica. Mentre queste applicazioni sono ancora in fase di sviluppo, i progressi nella costruzione di cellule sintetiche ci avvicinano sempre di più a un futuro in cui la biotecnologia avrà un ruolo centrale nel miglioramento della nostra salute e del nostro ambiente.
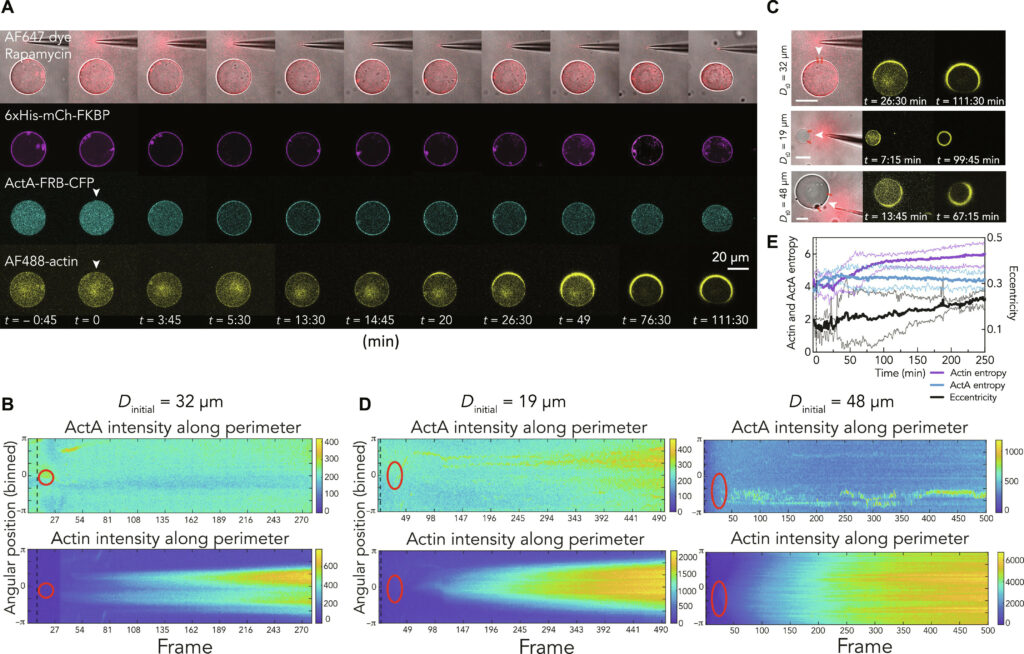
(A) Immagini confocali delle GUV durante la somministrazione di rapamicina. Al rilascio della rapamicina (contrassegnato dal segnale rosa del colorante Alexa Fluor 647), ActA trasloca dapprima nel punto contrassegnato dalla freccia bianca. La F-actina locale appare nello stesso sito entro ∼15 min. (B) Kymographs che mostrano l'evoluzione dell'intensità del segnale di ActA e actina sulla membrana per la GUV presentata in (A). L'ovale rosso indica l'area ad alta concentrazione effettiva di rapamicina. (C) Confronto dell'ispessimento dell'actina rispetto alla diffusione, per GUV di diverso raggio. L'area tra le due linee evidenzia l'area efficace di rapamicina. Barre di scala, 20 μm. (D) Simile a (B), ma mostra un chimografo dell'accumulo di segnale per le GUV di 48 e 19 μm rappresentate in (C). Il tempo 0 corrisponde all'aggiunta di rapamicina. (E) Grafici dell'entropia dei parametri di confine nel tempo, che evidenziano come l'entropia di ActA rimanga costante, mentre quella dell'actina e dell'eccentricità subiscano entrambe un picco dopo l'aggiunta di rapamicina. Le barre di errore indicano la SD. La linea nera tratteggiata segna il punto di aggiunta dell'input. Le immagini sono acquisite alla frequenza di un fotogramma al minuto.
Razavi, S., Wong, F., Abubaker-Sharif, B., Matsubayashi, H. T., Nakamura, H., Nguyen, N. T. H., … Inoue, T. (2024). Synthetic control of actin polymerization and symmetry breaking in active protocells. Science Advances, 10(24), eadk9731. doi:10.1126/sciadv.adk9731
In conclusione…
La cellula sintetica che si adatta rappresenta un importante passo avanti verso nuove frontiere biomediche. La sua capacità di imitare la flessibilità delle cellule naturali e la rottura della simmetria, fenomeno fondamentale per la vita, aprono la strada a nuove possibilità nella costruzione di organismi artificiali. I progressi nella costruzione di cellule sintetiche, dalla creazione del primo batterio al movimento cellulare, testimoniano l’evoluzione della ricerca in questo campo. Le proteine guida della riorganizzazione cellulare sono fondamentali per comprendere i meccanismi che regolano l’adattamento delle cellule sintetiche. Queste scoperte aprono la strada a nuove applicazioni nel campo della somministrazione di farmaci e del rilevamento ambientale. Tuttavia, rimane ancora molto da scoprire e da comprendere su queste cellule sintetiche e le loro potenziali implicazioni etiche e sociali. Cosa ci riserva il futuro nel campo delle cellule sintetiche? Quali saranno le conseguenze di questa nuova frontiera biomedica?





